MENÜ
DE | EUR
DE | EUR
-
- Alle Zentrifugen
- Tischzentrifugen
- Standzentrifugen
- Kühlzentrifugen
- Mikrozentrifugen
- Mehrzweckzentrifugen
- Hochgeschwindigkeitszentrifugen
- Ultrazentrifugen
- Concentrator
- IVD-Produkte
- Verbrauchsartikel für Hochgeschwindigkeits- und Ultrazentrifugen
- Zentrifugenröhrchen
- Zentrifugenplatten
- Gerätemanagement-Software
- Proben- und Informationsmanagement
-
- Alle Pipetten, Dispenser und automatischen Liquid-Handling-Systeme
- Mechanische Pipetten
- Elektronische Pipetten
- Mehrkanalpipetten
- Direktverdrängerpipetten und Dispenser
- Pipettenspitzen
- Flaschendispenser
- Pipettierhilfen
- Zubehör für Dispenser und Pipetten
- Automatisches Pipettieren
- Verbrauchsartikel für die Automation
- Zubehör für die Automation
- Services für Liquid-Handling-Geräte und Pipetten
Sorry, we couldn't find anything on our website containing your search term.
Sorry, we couldn't find anything on our website containing your search term.

Datentransfer in der Zelle
Beyond Science
- Lab Life
- Off the Bench
- Bright Minds
Die mRNA ist kein langes Molekül, sondern ein rundes Gebilde, fand der Wiener Forscher Clemens Plaschka heraus. Und nicht nur das.
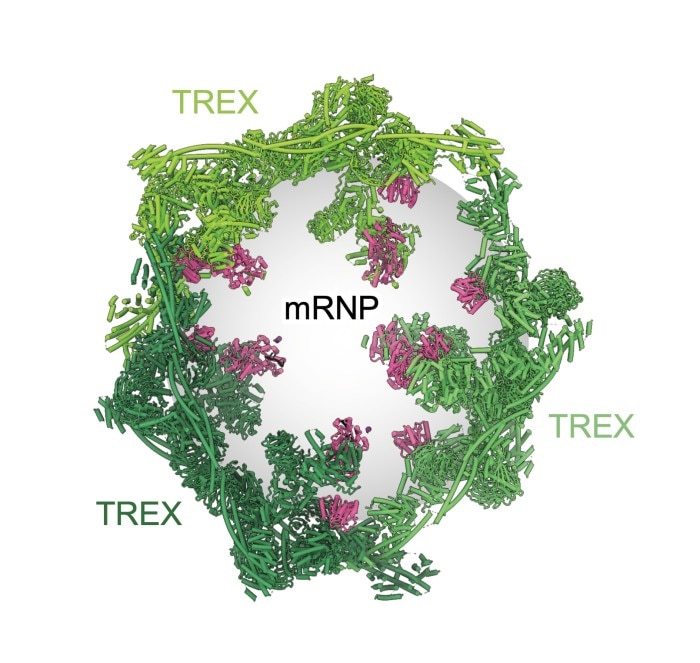
Spätestens seit der Coronapandemie ist die mRNA den meisten Menschen ein Begriff. Doch sie ist weit mehr als ein im Labor entworfener Impfstoff. Sie ist der universelle Bauplan für die Produktion von lebenswichtigen Proteinen in der Zelle. Aber wie sieht das lebenswichtige Transportmolekül überhaupt aus? Bisher wurde die Boten-RNA in Biologiebüchern als fadenförmig und langgestreckt abgebildet. „Eigentlich wusste das Forschungsfeld, dass das so nicht sein kann. Aber in Ermangelung eines besseren Modells hat man diese Vorstellung beibehalten“, erzählt Clemens Plaschka, dessen wissenschaftliche Arbeit erstmals visuelle Abbilder der Messenger-RNA liefert. Tatsächlich zeigen diese statt einer verschnörkelten Linie eine kompakte kugelförmige Struktur. „Unsere Arbeit aktualisiert die Lehrbuchansicht der mRNA, und das hat viele Auswirkungen: auf die mRNA-Biogenese, also wie die mRNA entsteht, den Transport der genetischen Informationen sowie den Zerfall der Moleküle, nachdem sie die Informationen für den Aufbau der Proteine ins Zytoplasma geliefert haben“, verrät der promovierte Biochemiker vom Research Institute of Molecular Pathology (IMP) in Wien.
Blackbox in der Molekularbiologie
Doch zunächst etwas Basiswissen: In der DNA liegen alle Informationen, die eine Zelle für den Aufbau benötigt, verschlüsselt und gespeichert im Inneren ihres Kerns. Für die Genexpression – umgangssprachlich: für den Export dieser Daten – fungiert die mRNA als Bote, der die in den Genen gespeicherten Proteinbaupläne abliest und dann auch noch aus dem Zellkern ins Zytoplasma transportiert. Das Zytoplasma ist die zelluläre Struktur, in der die komplexen Proteinmoleküle schließlich hergestellt werden. Ohne Proteine ist kein Leben möglich. Deshalb ist dieser mehrstufige Prozess von großer Bedeutung.
Wie Zellen sich organisieren, damit nur die korrekt gereifte Boten-RNA den Zellkern verlässt, war bis dato eine echte Blackbox in der Molekularbiologie. Über einen Zeitraum von fünf Jahren untersuchten Plaschka und sein Team, wie die richtige Messenger-RNA identifiziert und für den Export aus dem Nukleus präpariert wird. Dabei konnten sie nicht nur erstmals die Boten-RNA visualisieren und so zeigen, dass die mRNA kompakte dreidimensionale Kügelchen bildet, bevor sie den Zellkern verlässt. Sie konnten dank modernster Kryoelektronenmikroskopie auch herausfinden, wie sich das sogenannte Spleißosom, eine Art Molekülmaschine, wieder in seine Einzelteile zerlegt, nachdem sein Job erledigt ist und die mRNA für die Proteinproduktion modifiziert wurde. „Dabei haben wir festgestellt“, sagt Laborchef Plaschka, „dass die Demontage erst eintritt, wenn es ein ausgeklügelter Sicherheitsmechanismus erlaubt.“ Dabei handele es sich um einen komplizierten Prozess, „vergleichbar einer Multi-Faktor-Authentifizierung wie in der IT-Sicherheit“.
Glücksgefühl am Gipfelkreuz
Ein echter wissenschaftlicher Durchbruch, mit dem der zweisprachig in Wien und Chicago aufgewachsene Nachwuchsforscher selbst nicht gerechnet hat. „Aber ich liebe eben Challenges, in die man sich richtig hineinbeißen kann“, so der 35-Jährige. Ein schwieriges Problem ordentlich zu lösen, sei wie Bergsteigen: Oben am Gipfelkreuz angekommen, mache sich erst nach langem Aufstieg ein warmes Glücksgefühl breit. Seinen Forscherdrang führt Plaschka unter anderem auf seine Kindheit und die Schulzeit zurück. Die Leidenschaft für die Naturwissenschaften hätten „zwei wirklich tolle Lehrer, einer für Biologie, der andere für Chemie“, im Schulabschlussjahr geweckt, sodass er sich für das Studium der Biochemie entschied. Dort entdeckte er die Erklärungsfähigkeit der Strukturbiologie, die es erlaubt, Moleküle in 3D darzustellen. „Das fand ich total spannend“, erinnert sich Plaschka, zumal er als Fan von dreidimensionalen Videospielen dank der neuen Methode wissenschaftliche Themen nun auch dreidimensional angehen konnte. „Wissenschaftliche Probleme wurden so für mich einfach greifbar“, sagt er gestikulierend.
Schnell faszinierten Plaschka die vielen Unbekannten im Bereich der Genexpression. „Sie alle drehten sich um den Nukleus, also den Bereich, wo die DNA liegt und die mRNA produziert wird“, so der Forscher. Sein Vater, Wirtschaftsprofessor in den USA, habe schon früh seine Lust am rationalen Argumentieren geweckt: „Mein Bruder und ich mussten immer versuchen, ein noch besseres Argument in der Diskussion zu finden.“ Unabhängiges Denken und damit bisweilen auch eine unkonventionelle Herangehensweise habe sein Vater sehr gefördert. Wahrscheinlich, so mutmaßt Plaschka, habe er sich deshalb auch dieses an sich so sperrigen Themas angenommen. „Es motiviert mich, wissenschaftliche Probleme, die ich für groß halte, zu lösen und wirklich schwierige Fragen zu beantworten.“
Fragen über Fragen
Seinen wissenschaftlichen Beitrag versteht Clemens Plaschka übrigens als Grundlagenforschung, die das Feld nicht abschließend beantwortet, sondern „neue Felder öffnet“. „Ein wichtiges Resultat beeinflusst das Denken des Feldes“, resümiert Plaschka. Das Feld, die Zellbiologie, ist groß und vieles darin noch unklar. Zwar ist bekannt, wie dieses kleine Loch aussieht, durch das die Boten-RNA sich aus dem Zellkern durch die Zellmembran ins Zytoplasma schleust. „Aber wir haben noch keine gute Vorstellung davon, wie die RNA durch dieses kleine Loch hindurchgelangt“, erklärt Plaschka. Wandelt sie sich von einer Kugel- in eine lange Schlangenform? Und wie kann es sein, dass dieser Transfer immer nur in eine Richtung – vom Nukleus zum Zytoplasma – verläuft? Plaschka: „Mir geht es darum, dass wir diese Prozesse besser verstehen, die so essenziell für das Leben eines Menschen sind.“
Blackbox in der Molekularbiologie
Doch zunächst etwas Basiswissen: In der DNA liegen alle Informationen, die eine Zelle für den Aufbau benötigt, verschlüsselt und gespeichert im Inneren ihres Kerns. Für die Genexpression – umgangssprachlich: für den Export dieser Daten – fungiert die mRNA als Bote, der die in den Genen gespeicherten Proteinbaupläne abliest und dann auch noch aus dem Zellkern ins Zytoplasma transportiert. Das Zytoplasma ist die zelluläre Struktur, in der die komplexen Proteinmoleküle schließlich hergestellt werden. Ohne Proteine ist kein Leben möglich. Deshalb ist dieser mehrstufige Prozess von großer Bedeutung.
Wie Zellen sich organisieren, damit nur die korrekt gereifte Boten-RNA den Zellkern verlässt, war bis dato eine echte Blackbox in der Molekularbiologie. Über einen Zeitraum von fünf Jahren untersuchten Plaschka und sein Team, wie die richtige Messenger-RNA identifiziert und für den Export aus dem Nukleus präpariert wird. Dabei konnten sie nicht nur erstmals die Boten-RNA visualisieren und so zeigen, dass die mRNA kompakte dreidimensionale Kügelchen bildet, bevor sie den Zellkern verlässt. Sie konnten dank modernster Kryoelektronenmikroskopie auch herausfinden, wie sich das sogenannte Spleißosom, eine Art Molekülmaschine, wieder in seine Einzelteile zerlegt, nachdem sein Job erledigt ist und die mRNA für die Proteinproduktion modifiziert wurde. „Dabei haben wir festgestellt“, sagt Laborchef Plaschka, „dass die Demontage erst eintritt, wenn es ein ausgeklügelter Sicherheitsmechanismus erlaubt.“ Dabei handele es sich um einen komplizierten Prozess, „vergleichbar einer Multi-Faktor-Authentifizierung wie in der IT-Sicherheit“.
Glücksgefühl am Gipfelkreuz
Ein echter wissenschaftlicher Durchbruch, mit dem der zweisprachig in Wien und Chicago aufgewachsene Nachwuchsforscher selbst nicht gerechnet hat. „Aber ich liebe eben Challenges, in die man sich richtig hineinbeißen kann“, so der 35-Jährige. Ein schwieriges Problem ordentlich zu lösen, sei wie Bergsteigen: Oben am Gipfelkreuz angekommen, mache sich erst nach langem Aufstieg ein warmes Glücksgefühl breit. Seinen Forscherdrang führt Plaschka unter anderem auf seine Kindheit und die Schulzeit zurück. Die Leidenschaft für die Naturwissenschaften hätten „zwei wirklich tolle Lehrer, einer für Biologie, der andere für Chemie“, im Schulabschlussjahr geweckt, sodass er sich für das Studium der Biochemie entschied. Dort entdeckte er die Erklärungsfähigkeit der Strukturbiologie, die es erlaubt, Moleküle in 3D darzustellen. „Das fand ich total spannend“, erinnert sich Plaschka, zumal er als Fan von dreidimensionalen Videospielen dank der neuen Methode wissenschaftliche Themen nun auch dreidimensional angehen konnte. „Wissenschaftliche Probleme wurden so für mich einfach greifbar“, sagt er gestikulierend.
Schnell faszinierten Plaschka die vielen Unbekannten im Bereich der Genexpression. „Sie alle drehten sich um den Nukleus, also den Bereich, wo die DNA liegt und die mRNA produziert wird“, so der Forscher. Sein Vater, Wirtschaftsprofessor in den USA, habe schon früh seine Lust am rationalen Argumentieren geweckt: „Mein Bruder und ich mussten immer versuchen, ein noch besseres Argument in der Diskussion zu finden.“ Unabhängiges Denken und damit bisweilen auch eine unkonventionelle Herangehensweise habe sein Vater sehr gefördert. Wahrscheinlich, so mutmaßt Plaschka, habe er sich deshalb auch dieses an sich so sperrigen Themas angenommen. „Es motiviert mich, wissenschaftliche Probleme, die ich für groß halte, zu lösen und wirklich schwierige Fragen zu beantworten.“
Fragen über Fragen
Seinen wissenschaftlichen Beitrag versteht Clemens Plaschka übrigens als Grundlagenforschung, die das Feld nicht abschließend beantwortet, sondern „neue Felder öffnet“. „Ein wichtiges Resultat beeinflusst das Denken des Feldes“, resümiert Plaschka. Das Feld, die Zellbiologie, ist groß und vieles darin noch unklar. Zwar ist bekannt, wie dieses kleine Loch aussieht, durch das die Boten-RNA sich aus dem Zellkern durch die Zellmembran ins Zytoplasma schleust. „Aber wir haben noch keine gute Vorstellung davon, wie die RNA durch dieses kleine Loch hindurchgelangt“, erklärt Plaschka. Wandelt sie sich von einer Kugel- in eine lange Schlangenform? Und wie kann es sein, dass dieser Transfer immer nur in eine Richtung – vom Nukleus zum Zytoplasma – verläuft? Plaschka: „Mir geht es darum, dass wir diese Prozesse besser verstehen, die so essenziell für das Leben eines Menschen sind.“
Mehr erfahren
Zur Person
Clemens Plaschka, Jahrgang 89, studierte Biochemie in London, promovierte an der Universität in München und am Max-Planck-Institut für biophysikalische Chemie im Labor von Patrick Cramer zu strukturellen Grundlagen der Genaktivierung. Im Anschluss war er als Postdoktorand bei Kiyoshi Nagai am MRC Laboratory of Molecular Biology in Cambridge. Seit 2018 leitet er am Research Institute of Molecular Pathology (IMP) in Wien ein 15-köpfiges Team im eigenen Labor. Plaschka wurde mit mehreren Preisen ausgezeichnet und diversen Forschungsstipendien unterstützt, zuletzt erhielt er den Eppendorf Award 2024 für Nachwuchswissenschaftler. Die Preisverleihung fand am 27. Juni 2024 in Heidelberg statt.
Clemens Plaschka, Jahrgang 89, studierte Biochemie in London, promovierte an der Universität in München und am Max-Planck-Institut für biophysikalische Chemie im Labor von Patrick Cramer zu strukturellen Grundlagen der Genaktivierung. Im Anschluss war er als Postdoktorand bei Kiyoshi Nagai am MRC Laboratory of Molecular Biology in Cambridge. Seit 2018 leitet er am Research Institute of Molecular Pathology (IMP) in Wien ein 15-köpfiges Team im eigenen Labor. Plaschka wurde mit mehreren Preisen ausgezeichnet und diversen Forschungsstipendien unterstützt, zuletzt erhielt er den Eppendorf Award 2024 für Nachwuchswissenschaftler. Die Preisverleihung fand am 27. Juni 2024 in Heidelberg statt.
Mehr erfahren
Seine Forschung kompakt
In allen eukaryotischen Zellen – also in Zellen, die einen Zellkern aufweisen – sind die Transkription des Genoms und die Translation des Erbguts räumlich getrennt. Der erste Prozess ist im Zellkern zu verorten. Die Übersetzung der genetischen Baupläne in die Proteinproduktion, die Translation, findet aber im Zytoplasma statt, einer zellulären Grundstruktur außerhalb des Zellkerns. Diese Trennung ist für den sauberen genetischen Datenexport wichtig. Clemens Plaschka und sein Team am Wiener IMP haben durch die Kombination von „in vitro“-Ansätzen mit Zellkernextrakten (sowohl des Fadenwurms als auch von menschlichem Gewebe) neue Einblicke in die mRNA-Verpackung und den mRNA-Export geliefert. Dank modernster Kryoelektronenmikroskopie und Tomographie konnten sie erstmals visuelle Abbilder bestimmter Stadien liefern. Die Studie wurde unter anderem in der Zeitschrift „Nature“ veröffentlicht.
In allen eukaryotischen Zellen – also in Zellen, die einen Zellkern aufweisen – sind die Transkription des Genoms und die Translation des Erbguts räumlich getrennt. Der erste Prozess ist im Zellkern zu verorten. Die Übersetzung der genetischen Baupläne in die Proteinproduktion, die Translation, findet aber im Zytoplasma statt, einer zellulären Grundstruktur außerhalb des Zellkerns. Diese Trennung ist für den sauberen genetischen Datenexport wichtig. Clemens Plaschka und sein Team am Wiener IMP haben durch die Kombination von „in vitro“-Ansätzen mit Zellkernextrakten (sowohl des Fadenwurms als auch von menschlichem Gewebe) neue Einblicke in die mRNA-Verpackung und den mRNA-Export geliefert. Dank modernster Kryoelektronenmikroskopie und Tomographie konnten sie erstmals visuelle Abbilder bestimmter Stadien liefern. Die Studie wurde unter anderem in der Zeitschrift „Nature“ veröffentlicht.
Mehr erfahren
